اطلاعات پروژه
- دسته بندی: منومرها
جزئیات پروژه
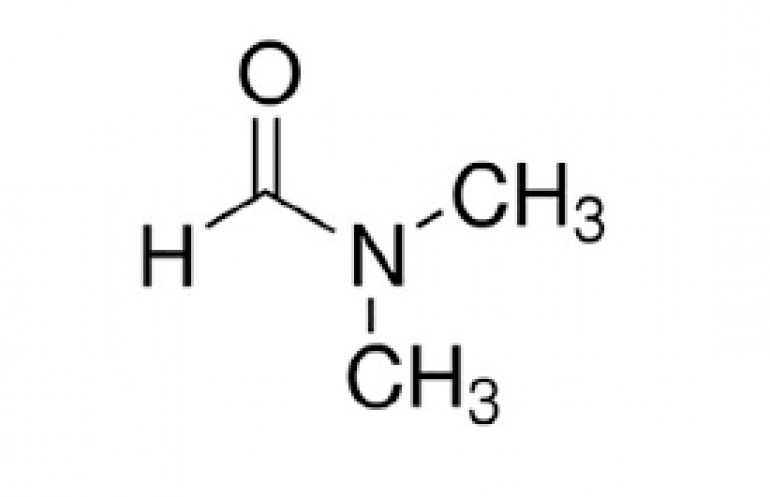
دیمتیل فرمآمید (به انگلیسی: Dimethylformamide) با فرمول شیمیایی C۳H۷NO یک ترکیب آلی با شناسه پابکم ۶۲۲۸ است. که جرم مولی آن 73.09 g/mol میباشد. شکل ظاهری این ترکیب، مایع شفاف است. بهطور معمول به صورت DMF (اگرچه DMF برای دی متیل فوران و یا دی متیل فومارات استفاده میشود)، این مایع بدون رنگ با آب و اکثر مایعات آلی میتواند مخلوط شود. DMF یک حلال رایج برای واکنشهای شیمیایی است. دی متیل فرمالید بیبو است، در حالیکه نمونههای فنی یا تخریب شده به دلیل ناخالصی از دیمتیل آمین اغلب دارای بوی ماهی هستند. ناخالصیهای تخریب دیمتیل آمین را میتوان با انجماد نمونههای تجزیه شده با گاز بی اثر مانند آرگون و یا سونیک کردن نمونههای تحت فشار کاهش یافته حذف کرد. عنوان نام آن نشان میدهد، این مشتق از فرمامید، آمیدِ اسید فرمیک است. DMF یک حلال پروتونی قطبی (هیدروفیل) با نقطه جوش بالا است و واکنشهایی که مکانیسمهای قطبی را دنبال میکند مانند واکنش جانشینی هستهدوستی دومولکولی تسهیل میکند.
جزئیات بیشتر در مورد پروژه
دیمتیل فرمآمید (به انگلیسی: Dimethylformamide) با فرمول شیمیایی C۳H۷NO یک ترکیب آلی با شناسه پابکم ۶۲۲۸ است. که جرم مولی آن 73.09 g/mol میباشد. شکل ظاهری این ترکیب، مایع شفاف است. بهطور معمول به صورت DMF (اگرچه DMF برای دی متیل فوران و یا دی متیل فومارات استفاده میشود)، این مایع بدون رنگ با آب و اکثر مایعات آلی میتواند مخلوط شود. DMF یک حلال رایج برای واکنشهای شیمیایی است. دی متیل فرمالید بیبو است، در حالیکه نمونههای فنی یا تخریب شده به دلیل ناخالصی از دیمتیل آمین اغلب دارای بوی ماهی هستند. ناخالصیهای تخریب دیمتیل آمین را میتوان با انجماد نمونههای تجزیه شده با گاز بی اثر مانند آرگون و یا سونیک کردن نمونههای تحت فشار کاهش یافته حذف کرد. عنوان نام آن نشان میدهد، این مشتق از فرمامید، آمیدِ اسید فرمیک است. DMF یک حلال پروتونی قطبی (هیدروفیل) با نقطه جوش بالا است و واکنشهایی که مکانیسمهای قطبی را دنبال میکند مانند واکنش جانشینی هستهدوستی دومولکولی تسهیل میکند.
محتویات
ساختار و ویژگیها
DMF در حضور بازهای قوی مثل سدیم هیدروکسید و اسیدهای قوی مثل HCl ,H2SO4 پایدار نیست و به فرمیک اسید و دی متیل آمین مخصوصاً با بالابردن دما هیدرولیز میشود . DMF به هر نسبتی در آب قابل امتزاج است . خالصسازی و خشک کردن DMF : DMF در دمای اتاق به آهستگی و در رفلاکس با سرعت بیشتری تخریب شده و دی متیل آمین و کربن مونو اکسید آزاد میکند . تخریب این ماده توسط ناخالصیهای اسیدی یا بازی تسریع میشود . قرار دادن DMF در واکنشگرهای خشک کن مثل کلسیم هیدرید یا سدیم هیدروکسید برای چند ساعت در دمای اتاق منجر به تخریب قابل توجه آن میگردد . خشک کردن DMF میتواند با خشک کردن توسط باریم اکسید(BaO) یا غربالهای مولکولی 4A در طول شب وسر ریز کردن ماده عاری از آب انجام شود . همچنین خالصسازی و خشک کردن با تقطیر در خلا در فشار حدود 20 mmHg انجام میشود و میتوان آن را در غربالهای 4A ذخیره کرد .
واکنشها
DMF توسط اسیدها و پایههای قوی، به خصوص در دمای بالا، هیدرولیز میشود. با استفاده از سدیم هیدروکسید، DMF به شکل دیمتیلآمین و فرمات تبدیل میشود. DMF در نزديكي نقطه جوش خود با دیکربونیلاسیون تبدیل به دیمتیلآمین میشود. بنابراین تقطیر تحت فشار کاهش یافته در دمای پایین انجام میشود.
در یکی از کاربردهای اصلی آن در سنتز آلی، DMF یک واکنشگر در واکنش Vilsmeier–Haack است که برای تشکیل ترکیبات آروماتیک استفاده میشود. [11] [12] این فرآیند شامل تبدیل اولیه DMF به یون کلرو ایمینیم، +[(CH3) 2N = CH (Cl)]، که به عنوان واکنشگر Vilsmeier شناخته میشود، که به هیدروکربنهای آروماتیک(arenes) حمله میکند.
ترکیبات ارگانولیتیم با DMF واکنش نشان میدهند و پس از هیدرولیز، آلدئیدها به دست میآیند.
تولید و ساخت
DMF برای اولین بار در سال 1893 توسط آلبرت ورلی، شیمیدان فرانسوی، بهوسیله مخلوطی از دیمتیلآمین هیدروژن کلرید و پتاسیم فرمات تهیه شد.
DMF با ترکیب متیل فرمات و دیمتیلآمین یا با واکنش دیمتیلآمین با مونوکسید کربن نیز تهیه میشود.
اگر چه در حال حاضر غیر عملی است، DMF را میتوان از دی اکسید کربن فوق بحرانی با استفاده از کاتالیزورهای مبتنی بر روتنیم تهیه کرد.
کاربردها
- مونومر پایه در تولید فیلم پلی آمیدی
- صنایع چسب و عایقکاری
- نقش واکنشگر در واکنشهای فرمیل دار کردن (Formylation reaction)
- نقش کاتالیزور در فرآیند تبدیل کربوکسیلیک اسیدها (carboxylic acids) به اسید کلراید ها (acid chlorides)
- حلال در بسیاری از واکنشهای شیمیایی
- صنایع نساجی و در بخش نخ ریسی آکریلیک و رنگرزی
- حلال مورداستفاده در صنایع دارویی
- در ساخت غشای نانو کامپوزیتی برای فرایندهای تصفیه آب